MUI Keluarkan Fatwa Vaksin Zivifax dari Anhui China Halal

Merdeka.com - Ketua Majelis Ulama Indonesia (MUI) Bidang Fatwa, Asrorun Ni’am Sholeh menetapkan fatwa Nomor 53 Tahun 2021 tentang Produk Vaksin Covid-19 dari Anhui Zhifei Longcom, China yaitu Zivifax hukumnya suci halal. Keputusan itu diambil setelah Komisi Fatwa MUI melakukan serangkaian penelitian dan pengkajian secara syar'i.
"Pertama, Vaksin Zivifax hukumnya suci dan halal. Kenapa? Karena dalam proses produksinya memenuhi standar halal dan tidak ditemukan penggunaan material yang haram dan atau najis," kata Asrorun dalam konferensi pers di Kantor MUI, Menteng, Jakarta, Sabtu (9/10).
Dalam telaahan tim auditor LPOM Komisi Fatwa MUI, papar Asrorun, proses produksi Vaksin Zivifax tidak ditemukan pemanfaatan barang haram dan atau najis, dalam ingredients dan juga dalam proses produksinya.
-
Siapa yang terlibat dalam produksi vaksin dalam negeri? Salah satu proyek unggulannya adalah pengembangan Vaksin Merah Putih atau INAVAC yang bekerja sama dengan Universitas Airlangga (Unair).
-
Apa tujuan produksi vaksin dalam negeri? Kemandirian dalam produksi vaksin merupakan salah satu kebijakan utama Kementerian Kesehatan (Kemenkes) dalam meningkatkan ketahanan kesehatan nasional.
-
Kapan vaksin Mpox mulai digunakan di Indonesia? Pelaksanaan vaksinasi Mpox dengan MVA-BN sudah dilakukan sejak 2023, setelah ditemukannya kasus konfirmasi Mpox di Indonesia.
-
Bagaimana cara meningkatkan ketahanan kesehatan melalui vaksin? Menkes Budi juga menambahkan, untuk mendukung ketahanan kesehatan, diperlukan penelitian yang berkelanjutan dan mengikuti perkembangan teknologi. Pemerintah melalui berbagai program terus mendorong pengembangan vaksin berbasis teknologi terkini.
-
Bagaimana penanganan Covid-19 di Indonesia? Jokowi memilih menggunakan strategi gas dan rem sejak awal untuk menangani pandemi Covid-19. Gas dan rem yang dimaksudkan Jokowi diimplementasikan dalam tiga strategi yakni penanganan kedaruratan kesehatan, jaring pengaman sosial, dan pemulihan ekonomi. Inilah yang kemudian menjadi ujung tombak dalam penanganan Covid-19 di Indonesia.
-
Kenapa vaksin Mpox diizinkan di Indonesia? Penggunaan vaksin Mpox di Indonesia kini telah mendapat persetujuan dari Organisasi Kesehatan Dunia (WHO) dan Badan Pengawas Obat dan Makanan (BPOM) RI, yang menunjukkan bahwa vaksin ini aman dan dapat digunakan dalam kondisi darurat kesehatan.
"Sebagaimana mekanisme yang sudah ditetapkan di MUI, dokumen-dokumen untuk kepentingan pemfatwaan Vaksin Zivifax juga telah diverifikasi oleh tim dan selanjutnya dilakukan pemeriksaan," ujarnya.
Baik pemeriksaan berbasis dokumen, lanjut Asrorun, maupun pemeriksaan berbasis kunjungan lapangan atau audit langsung dengan visitasi yang dilakukan oleh tim auditor ke pabrik Zhifei Longcom Biopharmaceutical Co, Ltd di Hefei, China.
"Baik pada aspek teknis, ingredients berikut pada proses produksi maupun aspek syar'inya. Kedua, Vaksin Covid-19 produk Anhui sebagaimana angka satu, boleh digunakan dengan syarat terjamin keamanannya menurut ahli atau lembaga yang kompeten," jelasnya.
Ia menegaskan, pada point kedua tersebut menjadi penting. Karena, kebolehan penggunaan Vaksin Zivifax terikat oleh aspek ketoyiban, aspek keamanan juga efikasi.
MUI berharap, rekomendasinya memiliki kesamaan pandang dengan pemerintah terkait komitmen penanggulangan Covid-19. Salah satunya dengan perluasan akses terhadap vaksin bagi masyarakat.
"Alhamdulillah dengan adanya satu produk yang memenuhi halal dan toyib sebagaimana ditetapkan juga oleh Badan POM, maka MUI mengharapkan pemerintah terus mengikhtiarkan dengan memprioritaskan pengadaan vaksin yang halal semaksimal mungkin," ucapnya.
MUI berharap rekomendasinya tidak dipersepsikan miring, namun lebih semata untuk kepentingan dan komitmen bersama dalam rangka menjaga, melindungi dan merawat kesehatan masyarakat.
Hal itu dilakukan dengan menjaga prokes, meningkatkan cakupan vaksin, menyediakan vaksin yang halal dan toyib. Sehingga vaksinasi dapat dilakukan secara optimal sesuai dengan keyakinan keagamaan dan sesuai aspek keamanan dalam penggunaannya.
"Fatwa ini adalah jawaban hukum Islam, maka pendekatannya adalah pendekatan hukum Islam didalam menetapkan fatwanya," ungkapnya.
Sementara itu, Director of Marketing and Partnerships PT. Jakarta Biopharmaceutical Industry (JBio) Chairuddin Yunus MKes menyampaikan rasa syukurnya atas Vaksin Zivifax yang diproduksi oleh Anhui Zhifei Longcom Biopharmaceutical asal Tiongkok dan dikembangkan di Indonesia dengan bekerjasama dengan JBio dinyatakan halal oleh MUI.
"Kami sangat bersyukur Zivifax dinyatakan halal oleh MUI. Semoga kerja keras kami dalam memproduksi vaksin dan melalui proses panjang pengujian dapat bermanfaat untuk Indonesia dalam mempercepat vaksinasi Covid-19," ujar Chairuddin.
Uji klinik vaksin Zivifax di Indonesia disebutnya dilaksanakan di Jakarta dan di Bandung dengan 4.000 subjek. Kapasitas produksi produsen sekitar 200–300 juta dosis vaksin Covid-19 untuk produk jadi dan 1 miliar dosis untuk produk setengah jadi.
"Produsen berkomitmen untuk dapat menyuplai 50 juta dosis untuk pemerintah Indonesia di tahun ini. Untuk tahun 2022, Produsen berkomitmen untuk menyuplai 20 – 25 juta dosis per bulan untuk pemerintah Indonesia," katanya.
"Selain target menyuplai vaksin, kami juga berkomitmen melakukan transfer teknologi agar Zivifax dapat diproduksi di dalam negeri oleh putra-putri Indonesia," sambungnya.
Sebelumnya, Badan Pengawas Obat dan Makanan (BPOM) menerbitkan izin penggunaan darurat atau Emergency Use Authorization (UEA) untuk vaksin Zivifax sebagai salah satu vaksin mencegah penularan Covid-19. Vaksin ini dikembangkan Anhui Zhifei Longcom Biopharmaceutical.
"Pada hari ini BPOM kembali menginformasikan, telah diberikannya persetujuan terhadap satu produk vaksin covid-19 yang baru, dengan nama dagangnya Zivifax yang dikembangkan Anhui Zhifei Longcom Biopharmaceutical dan dikembangkan di Indonesia bekerjasama dengan PT JBio," ujar Kepala BPOM, Penny Kusumastuti Lukito, dalam konferensi pers BPOM, Kamis (7/10).
Penny menjelaskan, uji klinik telah dilakukan bersama sejumlah multi center beserta sejumlah subjeknya.
"Vaksin ini dikembangkan melalui uji klinik yang juga dilakukan di Indonesia. Ini adalah uji klinik yang dilakukan bersama-sama multi center ada Indonesia, ada di China juga fase tiganya, Pakistan, Uzbekistan, dan Ekuador. Dengan jumlah subjek sekitar 28.500 dan di Indonesia sendiri ada 4.000 subjek karena ini dilakukan dari Bandung ya, di Bandung dengan FK UI, RSCM Jakarta," kata Penny.
Kemudian, untuk uji fase 3, dilaksanakan di berbagai center di RSCM Jakarta, di FK Unpad Rumah Sakit Hasan Sadikin Bandung, dan di berbagai rumah sakit yang tersebar di Bandung serta beberapa Puskesmas yang tersebar di Jakarta.
"Jadi ini juga meningkatkan menambah kemampuan atau pengalaman Indonesia dalam uji vaksin. Dan juga akan dilakukan transteknologi ya. Saya kira itu adalah harapan kita semua bahwa ke depan kita akan terus mengembangkan kemampuan produksi dalam negeri, transfer teknologi tentunya dari produk-produk yang sudah dikembangkan di Indonesia dilakukan oleh industri farmasi BUMN maupun jaga industri Farmasi swasta dengan melakukan transfer teknologi," ujarnya.
Sekadar informasi, Zivifax menjadi vaksin Covid-19 kesepuluh yang diberikan izin penggunaan darurat di Indonesia. Vaksin ini dibuat menggunakan metode protein rekombinan, yakni menggunakan sebagian dari komponen virus untuk memicu reaksi imun tubuh. Metode itu dinilai lebih aman bagi pasien dengan masalah sistem imun (immunocompromised).
Setelah melalui studi klinik fase 1,2 dan 3, pemberian vaksin secara umum dapat ditoleransi dengan baik. Penny menjelaskan ada beberapa adverse effect atau efek yang bisa muncul usai mendapatkan vaksin ini. Seperti nyeri pada tempat suntikan, sakit kepala, kelelahan, demam.
Penny menambahkan, persentase efikasi vaksin ini yang mencapai lebih dari 80 persen.
"Efikasi berdasarkan interim studi uji klinis fase tiga yang baik. Efikasi mencapai 81,71 persen yang dihitung setelah 7 hari secara vaksinasi lengkap dan mencapai 81,4 persen setelah 14 hari vaksinasi lengkap. Vaksin ini diberikan dalam 3 kali suntikan dalam rentan 3 bulan," ujarnya.
(mdk/rhm)Cobain For You Page (FYP) Yang kamu suka ada di sini,
lihat isinya

Namun kalau untuk yang komorbid, kata Menkes, risiko tetap ada karena virusnya tidak hilang.
Baca Selengkapnya
Pembangunan pabrik yang berlokasi di Cikarang ini merupakan strategi global untuk memperkuat basis produksi dan distribusi produk.
Baca Selengkapnya
Jamie Scott, seorang pria beranak dua mengalami cedera otak serius setelah mengalami penggumpalan darah dan pendarahan di otak usai mendapatkan vaksin itu p
Baca Selengkapnya
Biofarma mengajukan Penyertaan Modal Negara (PMN) untuk tahun 2025 sebesar Rp2,21 triliun.
Baca Selengkapnya
Pemerintah mengimbau masyarakat untuk melakukan vaksinasi Covid-19 sampai dosis kelima atau booster ketiga.
Baca Selengkapnya
Pemerintah berupaya mencegah penyebaran Mpox dengan melakukan vaksinasi yang sudah disetujui WHO dan BPOM.
Baca Selengkapnya
Produksi vaksin dalam negeri dianggap akan mampu mendorong ketahanan kesehatan nasional.
Baca Selengkapnya
Penerima vaksin ini adalah laki-laki yang dalam dua minggu terakhir melakukan hubungan seksual berisiko dengan atau tanpa status ODHIV.
Baca Selengkapnya
Penemuan kasus yang dihimpun per tanggal 6-23 Desember 2023 sebanyak 5 kasus.
Baca Selengkapnya
Beberapa waktu terakhir terjadi lonjakan kasus Covid-19 yang cukup signifikan di Indonesia.
Baca Selengkapnya
Vaksin Nusagard akan digunakan pada Program Imunisasi Nasional pada 2023 mendatang. Program ini menyasar 2,9 juta anak usia kelas 5 dan 6 sekolah dasar (SD).
Baca Selengkapnya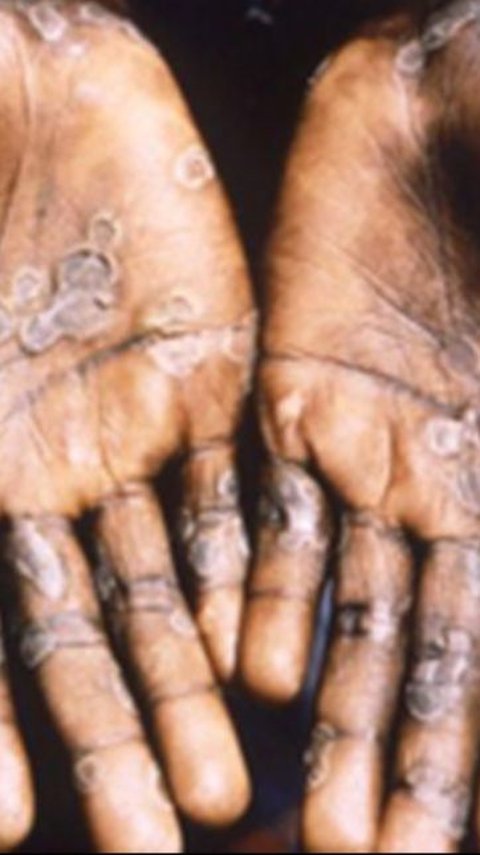
Kelompok orang yang rawan tertular cacar monyet diminta untuk sadar dalam mencegah penyakit ini.
Baca Selengkapnya